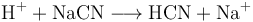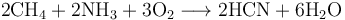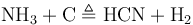氰化氢
(重定向自氢氰酸)
| A+医学百科 >> 氰化氢 |
| 氰化氢 | |
|---|---|
 |
|
| IUPAC名 Hydrogen cyanide |
|
| 别名 | 氢氰酸 |
| 识别 | |
| CAS号 | 74-90-8 |
| RTECS | MW6825000 |
| 性质 | |
| 化学式 | HCN |
| 摩尔质量 | 27.03 g·mol⁻¹ |
| 外观 | 无色气体或淡蓝色易挥发液体 |
| 密度 | (液) 0.687 |
| 熔点 | -13.4°C (259.75 K, 7.88°F) |
| 沸点 | 26°C (299.15 K, 78.8°F) |
| 溶解性(水) | 易溶 |
| pKa | 9.2 - 9.3 |
| 结构 | |
| 分子构型 | 直线形 |
| 偶极矩 | 2.98 D |
| 危险性 | |
| 警示术语 | R:R12-R26-R27-R28-R32 |
| 安全术语 | S:S1/2-S7-S9-S13-S16-S28-S29-S45 |
| 主要危害 | 剧毒及易燃 |
| NFPA 704 | |
| 闪点 | −17.78 °C |
| 相关物质 | |
| 相关化学品 | 氰、氯化氰、磷杂乙炔 三甲基氰硅烷 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
氰化氢,又称氢氰酸,化学式HCN。标准状态下为气体,剧毒且致命,无色而苦,并有杏仁气味,能否嗅出视乎个人基因[来源请求]。氰化氢是一种无色,有毒液体, 它是一种弱酸,沸点26℃(79°F)。氰化氢是一个线性分子,碳和氮之间具有三键。
目录 |
制取
氰化氢的实验室制法是通过氰化物与酸反应制备,如:
最重要的工业制取氰化氢的方法要数Andrussow氧化反应,它是通过甲烷、氨气以及氧气在约1200°C经由铂催化得到氰化氢:
- 其中反应所需能量由甲烷和氨气的部分氧化提供。
或者由石墨与氨气加强热生成气体,冷凝后得液体氰化氢。
化学性质
分子可溶于水中形成氢氰酸。可与卤代烃进行亲核取代反应(SN),及与羰基化合物进行亲核加成反应生成α-羟基腈。由于可以使化合物增加一个碳原子,故是重要的有机合成试剂和化工步骤,实际上常用CN−作亲核试剂。
危害
健康危害:抑制细胞色素氧化酶,造成细胞内窒息。可致眼、皮肤灼伤,吸收引起中毒。
急性中毒:
- 短时间内吸入高浓度氰化氢气体,可立即呼吸停止而死亡。
- 非骤死者临床分为4期:
- 前驱期有粘膜刺激、呼吸加快加深、乏力、头痛;口服有舌尖、口腔发麻等。
- 呼吸困难期有呼吸困难、血压升高、皮肤粘膜呈鲜红色等。
- 惊厥期出现抽搐、昏迷、呼吸衰竭。
- 麻痹期全身肌肉松弛,呼吸心跳停止而死亡。
参阅
参考资料
- ↑ Andrussow, L.. The catalytic oxydation of ammonia-methane-mixtures to hydrogen cyanide. Angewandte Chemie. 1935, 48 (37): 593–595. doi:10.1002/ange.19350483702.
外部链接
|
|||||||||||||||||||||||||||||||||||||||||||||||
参考来源
出自A+医学百科 “氰化氢”条目 http://www.a-hospital.com/w/%E6%B0%B0%E5%8C%96%E6%B0%A2 转载请保留此链接
| 关于“氰化氢”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |