过氧化氢酶
| A+医学百科 >> 过氧化氢酶 |
目录 |
简介
过氧化氢酶存在于红细胞及某些组织内的过氧化体中,它的主要作用就是催化H2O2分解为H2O与O2,使得H2O2不至于与O2在铁螯合物作用下反应生成非常有害的-OH
过氧化氢酶是过氧化物酶体的标志酶, 约占过氧化物酶体酶总量的40%。过氧化氢酶的作用是使过氧化氢还原成水: 2H2O2 → O2 + 2H2O
触酶
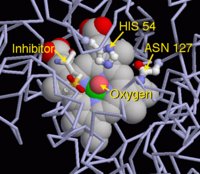
过氧化氢酶(CAT)是一种酶类清除剂,又称为触酶,是以铁卟啉为辅基的结合酶。它可促使H2O2分解为分子氧和水,清除体内的过氧化氢,从而使细胞免于遭受H2O2的毒害,是生物防御体系的关键酶之一。CAT作用于过氧化氢的机理实质上是H2O2的歧化,必须有两个H2O2先后与CAT相遇且碰撞在活性中心上,才能发生反应。H2O2浓度越高,分解速度越快。
来源
几乎所有的生物机体都存在过氧化氢酶。其普遍存在于能呼吸的生物体内,主要存在于植物的叶绿体、线粒体、内质网、动物的肝和红细胞中,其酶促活性为机体提供了抗氧化防御机理。
CAT是红血素酶,不同的来源有不同的结构。在不同的组织中其活性水平高低不同。过氧化氢在肝脏中分解速度比在脑或心脏等器官快,就是因为肝中的CAT含量水平高。
H2O2 分解酶
这是一种稳定的过氧化氢分解酶, 能将过氧化氢分解成水和氧气, 而对纤维和染料没有影响, 因而漂白后染色前, 通过H2O2 分解酶去除漂白织物上和染缸中残留的过氧化氢, 以避免纤维的进一步氧化和染色时染料的氧化。同时能缩短加工时间,减少水洗用水, 降低废水量。尤其对纱线、筒子纱和针织物更为适用。 同样, 过氧化氢分解酶随pH 值和温度的改变, 其活力随之变化, 在pH7 左右和30~40 ℃活性最大。过氧化氢浓度增大, 会加快分解反应速度, 但必须注意当浓度大于一定量时, 酶的作用将减弱, 这样过多的残留H2O2 对纤维和染料是不利的。所以不能因为有了H2O2 分解酶, 就能任意地加大H2O2 的用量。 使用时, 通常要注意H2O2 分解酶对常用表面活性剂和H2O2 稳定剂的相容性, 实际生产应用pH为6~8 , 温度20~55 ℃, 酶用量5~10KCLU/ 升,时间10~20min。此技术已慢慢地被国内所认识和接受, 它对提高活性染料色泽鲜艳度很有利。
酶可促进漂白
要说明的是用酶可促进漂白的进行, 羊毛在含有蛋白酶Bactosol ST的过氧化氢漂液中漂白, 可显著提高羊毛的白度和亲水性。这是由于酶促进羊毛纤维初始受到快速的浸蚀, 致使羊毛漂白较易进行。从此原理出发, 将蛋白酶对羊毛先预处理, 使纤维表面裸露, 再进行漂白, 显然效果更好, 且纤维损伤也易控制。
过氧化氢酶历史
作为一种物质,过氧化氢酶是在1811年被过氧化氢(H2O2)的发现者泰纳尔(Louis Jacques Thénard)首次发现。1900年,Oscar Loew将这种能够降解过氧化氢的酶命名为“catalase”,即过氧化氢酶,并发现这种酶存在于许多植物和动物中。1937年,詹姆斯.B.萨姆纳将来自牛肝中的过氧化氢酶结晶,并在次年获得了该酶的分子量。1969年,牛的过氧化氢酶的氨基酸序列得以解出。而后,1981年,其三维结构得以解析。
| 关于“过氧化氢酶”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |