生物化学与分子生物学/蛋白质的结构与功能的关系
| 医学电子书 >> 《生物化学与分子生物学》 >> 蛋白质化学 >> 蛋白质的结构及其功能 >> 蛋白质的结构与功能的关系 |
| 生物化学与分子生物学 |
|
|
蛋白质一级结构是空间结构的基础,特定的空间构象主要是由蛋白质分子中肽链和侧链R基团形成的次级键来维持,在生物体内,蛋白质的多肽链一旦被合成后,即可根据一级结构的特点自然折叠和盘曲,形成一定的空间构象。
Anfinsen以一条肽链的蛋白质核糖核酸酶为对象,研究二硫键的还原和氧化问题,发现该酶的124个氨基酸残基构成的多肽链中存在四对二硫键,在大量β-巯基乙醇和适量尿素作用下,四对二硫键全部被还原为桽H,酶活力也全部丧失,但是如将尿素和β-巯基乙醇除去,并在有氧条件下使巯基缓慢氧化成二硫键,此时酶的活力水平可接近于天然的酶。Anfinsen在此基础上认为蛋白质的一级结构决定了它的二级、三级结构,即由一级结构可以自动地发展到二、三级结构(图1-10)。
一级结构相似的蛋白质,其基本构象及功能也相似,例如,不同种属的生物体分离出来的同一功能的蛋白质,其一级结构只有极少的差别,而且在系统发生上进化位置相距愈近的差异愈小(表1-2,表1-3)。
表1-2 胰岛素分子中氨基酸残基的差异部分
| 胰岛素来源 | 氨基酸残基的差异部分 | |||
| A5 | A6 | A10 | A30 | |
| 人 | Thr | Ser | Ile | Thr |
| 猪 | Thr | Ser | Ile | Ala |
| 狗 | Thr | Ser | Ile | Ala |
| 兔 | Thr | Ser | Ile | Ser |
| 牛 | Ala | Ser | Val | Ala |
| 羊 | Ala | Gly | Val | Ala |
| 马 | Thr | Gly | Ile | Ala |
| 抹香猄 | Thr | Ser | Ile | Ala |
| 鲤猄 | Ala | Ser | Thr | Ala |
表1-3 细胞色素C分子中氨基酸残基的差异数目及分歧时间
| 不同种属 | 氨基酸残基的差异数目 | 分歧时间(百万年) |
| 人-猴 | 1 | 50-60 |
| 人-马 | 12 | 70-75 |
| 人-狗 | 10 | 70-75 |
| 猪-牛-羊 | 0 | |
| 马-牛 | 3 | 60-65 |
| 哺乳类-鸡 | 10-15 | 280 |
| 哺乳类-猢 | 17-21 | 400 |
| 脊椎动物-酵母 | 43-48 | 1,100 |
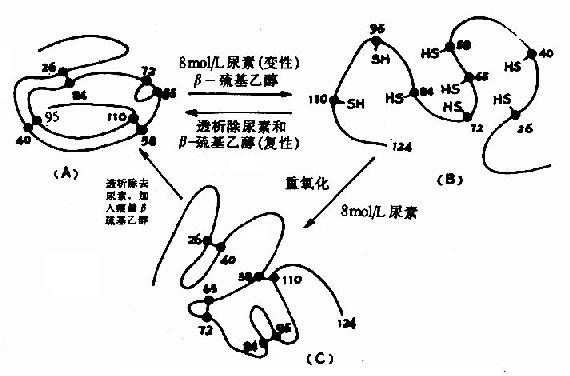
图1-11 核糖核酸酶的变性和复性示意图
(A)天然核糖核酸酶(B)变性失活(C)“错乱”核糖核酸酶
促肾上腺皮质激素(ACTH)和促黑激素(MSH)均为垂体分泌的多肽激素。α-MSH和ACTh 4~10位的氨基酸结构与β-MSH的11~17位一样,故ACTH有较弱的MSH的生理作用(图1-12)。
在蛋白质的一级结构中,参与功能活性部位的残基或处于特定构象关键部位的残基,即使在整个分子中发生一个残基的异常,那么该蛋白质的功能也会受到明显的影响。被称之为“分子病”的镰刀状红细胞性贫血仅仅是574个氨基酸残基中,一个氨基酸残基即β亚基N端的第6号氨基酸残基发生了变异所造成的,这种变异来源于基因上遗传信息的突变(如图1-13)。
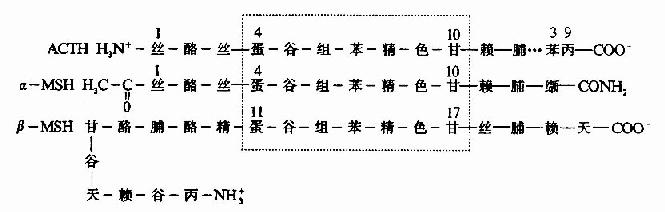
图1-12 ACTH、α-MSH和β-MSH一级结构比较
| 正常 | DNA | ……TGt GGG CTT CTT TTT…… |
| mRNA | ACA CCC GAA GAA AAA | |
| DNA(β亚基) | N端…苏-脯-谷-谷-赖…… | |
| 异常 | DNA | ……TGT GGG GAT CTT TTT…… |
| mRNA | ……ACa CCC GUA GAA AAA…… | |
| hbs(β亚基) | N端…苏-脯-缬-谷-赖…… |
图1-13 镰刀状红细胞性贫血血红蛋白遗传信息的异常
(二)蛋白质空间橡象与功能活性的关系
蛋白质多种多样的功能与各种蛋白质特定的空间构象密切相关,蛋白质的空间构象是其功能活性的基础,构象发生变化,其功能活性也随之改变。蛋白质变性时,由于其空间构象被破坏,故引起功能活性丧失,变性蛋白质在复性后,构象复原,活性即能恢复。
在生物体内,当某种物质特异地与蛋白质分子的某个部位结合,触发该蛋白质的构象发生一定变化,从而导致其功能活性的变化,这种现象称为蛋白质的别构效应(allostery)。
蛋白质(或酶)的别构效应,在生物体内普遍存在,这对物质代谢的调节和某些生理功能的变化都是十分重要的。
现以血红蛋白(hemoglobin,简写Hb)为例来说明构象与功能的关系。
血红蛋白是红细胞中所含有的一种结合蛋白质,它的蛋白质部分称为珠蛋白(globin),非蛋白质部分(辅基)称为血红素(见图1-14)。Hb分子由四个亚基构成,每一亚基结合一分子血红素。正常成人Hb分子的四个亚基为两条α链,两条β链。α链由141个氨基酸残基组成,β链由146个氨基酸残基组成,它们的一级结构均已确定。每一亚基都具有独立的三级结构,各肽链折叠盘曲成一定构象,β亚基中有8个α-螺旋区(分别称A、B……H螺旋区),α亚基中有7个α-螺旋区。在此基础上肽链进一步折叠形成球状,依赖侧链间形成的各种次级键维持稳定,使之球形表面为亲水区,球形向内,在E和F螺旋段间的20多个巯水氨基酸侧链构成口袋形的疏水区,辅基血红素就嵌接在其中,α亚基和β亚基构象相似,最后,四个亚基α2β2聚合成具有四级结构的Hb分子(见图1-15)。在此分子中,四个亚基沿中央轴排布四方,两α亚基沿不同方向嵌入两个β亚基间,各亚基间依多种次级健联系,使整个分子呈球形,这些次级键对于维系Hb分子空间构象有重要作用,例如在四亚基间的8对盐键(图1-16),它们的形成和断裂将使整个分子的空间构象发生变化。
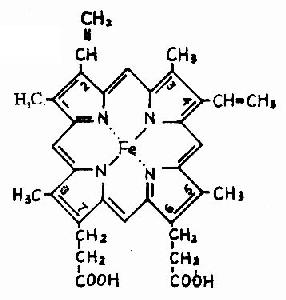
图1-14 血红素的结构式
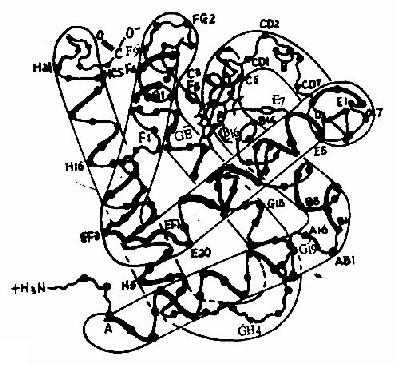
图1-15 血红蛋白β亚基的构象
ABCDEFGH分别代表不同的α-螺旋区。共有八个螺旋区;阿拉伯数字代表在该区氨基酸残基的序号;a-螺旋区之间的移行部位为无规卷曲,用AB,CD,EF,FG…等表示。C1,E7,C5,CF,C3,E3,的中间为血红素,其中较大的黑点代表Fe2+。
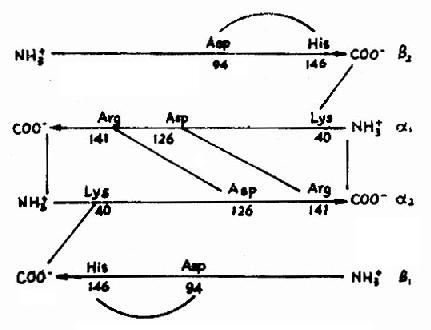
图1-16 血红蛋白亚基间盐键示意图
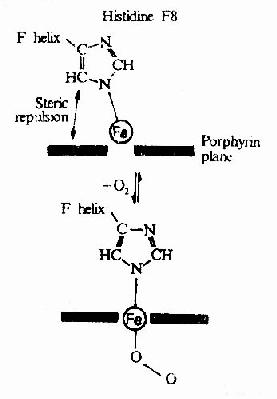
图1-7 铁原子在氧合时落入血红素平面
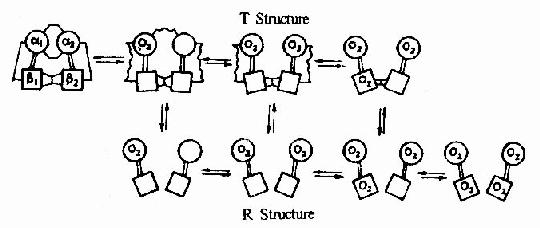
图1-18
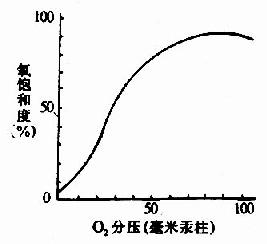
图1-19 Hb的氧饱和曲线
Hb在体内的主要功能为运输氧气,而Hb的别位效应,极有利于它在肺部与O2结合及在周围组织释放O2。
Hb是通过其辅基血红素的Fe++与氧发生可逆结合的,血红素的铁原子共有6个配位键,其中4个与血红素的吡咯环的N结合,一个与珠蛋白亚基F螺旋区的第8位组氨酸(F8)残基的咪唑基的N相连接,空着的一个配位键可与O2可逆地结合,结合物称氧合血红蛋白。
在血红素中,四个吡咯环形成一个平面,在未与氧结合时Fe++的位置高于平面0.7Å,一旦O2进入某一个α亚基的疏水“口袋”时,与Fe++的结合会使Fe++嵌入四吡咯平面中,也即向该平面内移动约0.75Å(图1-17),铁的位置的这一微小移动,牵动F8组氨酸残基连同F螺旋段的位移,再波及附近肽段构象,造成两个α亚基间盐键断裂,使亚基间结合变松,并促进第二亚基的变构并氧合,后者又促进第三亚基的氧合(图1-18)使Hb分子中第四亚基的氧合速度为第一亚基开始氧合时速度的数百倍。此种一个亚基的别构作用,促进另一亚基变构的现象,称为亚基间的协同效应(cooperativity),所以在不同氧分压下,Hb氧饱和曲线呈“S”型(图1-19)。
| 关于“生物化学与分子生物学/蛋白质的结构与功能的关系”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |