Β受体阻滞剂
| A+医学百科 >> Β受体阻滞剂 |
β受体阻滞剂是能选择性地与β肾上腺素受体结合、从而拮抗神经递质和儿茶酚胺对β受体的激动作用的一种药物类型。肾上腺素受体分布于大部分交感神经节后纤维所支配的效应器细胞膜上,其受体分为 3 种类型, 即β1受体、β2受体和β3受体。β1受体主要分布于心肌, 可激动引起心率和心肌收缩力增加;β2受体存在于支气管和血管平滑肌, 可激动引起支气管扩张、血管舒张、内脏平滑肌松弛等;β3受体主要存在于脂肪细胞上,可激动引起脂肪分解。这些效应均可被 β受体阻滞剂所阻断和拮抗。各种β阻滞剂的作用机制、不良反应和临床疗效差异很大,需要择优使用。
目录 |
分为三类
第一类为非选择性的,作用于β1和β2受体,常用药物为普萘洛尔(心得安),由于为非选择性,所以副作用较多,目前已较少应用;
第二类为选择性的,主要作用于β1受体,常用药物为美托洛尔(倍他乐克)、阿替洛尔(氨酰心安)、比索洛尔(康可)等;
第三类也为非选择性的,可同时作用于β和α1受体,具有外周扩血管作用,常用药物为卡维地洛、拉贝洛尔。
β受体阻滞剂还可以划分为脂溶性或水溶性,以及具有内在拟交感活性或不具有内在拟交感活性等类型。
β受体阻滞剂具有明显异质性,不同的β受体阻滞剂作用可能会不一样。β受体阻滞剂的异质性来自3种主要差异,包括心脏选择性(β1)、脂溶性及内在拟交感活性(ISA),这些差异可表达为死亡率的高低。此外,选择性的β1受体阻滞剂对β2受体影响较小,基本不会引起支气管痉挛或血糖血脂代谢紊乱。β受体阻滞剂的亲脂性是影响其疗效和安全性的重要因素,高亲脂性β受体阻滞剂具有明确的心脏保护作用,而低亲脂性的则没有。
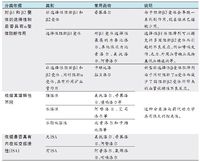
| 类别 | 特点 | 主要药物 | 临床特点 |
|---|---|---|---|
| β受体非选择性 | 同时阻滞β1和β2受体 | 索他洛尔、普萘洛尔 | 已经较少使用 |
| β1受体选择性 | 选择性阻滞β1受体,对β2受体影响甚微 | 奈必洛尔、美托洛尔、比索洛尔、阿替洛尔 | 可避免因为阻断β2受体而出现的副作用,比如哮喘发作、乏力、外周血管缺血及掩盖低血糖症状等 |
| 兼具α受体阻滞作用 | 选择性阻滞β1受体,兼具非选择性阻滞β/α受体,具有外周扩血管作用 | 卡维地洛、阿罗洛尔 | 减少了血管收缩性不良反应 |
β受体阻滞剂的治疗作用
- 高血压病:β受体阻滞剂适用于不同严重程度的高血压,尤其是心率较快的中青年患者,也适用于合并有心绞痛、心肌梗死后、快速心律失常、充血性心力衰竭和妊娠的高血压患者。
- 冠心病:β受体阻滞剂具有较强的降低心肌耗氧作用和拮抗儿茶酚胺的致心律失常作用,提高室颤阈,抗血小板和减轻心脏血管损害,降低心肌再梗死率,改善梗死后左室重构。
- 心力衰竭:大规模β受体阻滞剂实验证明,长期应用β受体阻滞剂,可降低心力衰竭患者总体死亡率、心血管病死亡率、心源性猝死以及心力衰竭恶化引起的死亡,通常从小剂量开始,逐渐加量以达到最大耐受剂量。但在有包括肺底啰音在内的多种体征的急性心力衰竭患者中使用β受体阻滞剂应慎重。
- 心律失常:β受体阻滞剂常用于快速性心律失常的治疗,包括窦速、房早、室早、房速、室上性心动过速及室速。
- 主动脉夹层:内科治疗常联合应用β受体阻滞剂和硝普钠,减少血流对主动脉的冲击,减少左心室的收缩速率以减缓病情进展。
- 心肌病:在有症状的肥厚性心肌病患者中,β受体阻滞剂是首选治疗,可控制心室率,降低心肌收缩力,使心室充盈及舒张末容量最大化,改善心肌顺应性。β受体阻滞剂用于扩张性心肌病伴或不伴心力衰竭的治疗,可减轻症状、预防猝死和改善预后。
- 遗传性QT延长综合征(LQTS):除非有严重的禁忌证,β受体阻滞剂是当今对有症状的LQTS患者的首选治疗。若无绝对禁忌证,推荐终身服用最大耐受剂量的β受体阻滞剂,可明显降低心血管事件的发生。目前认为,对于无症状的LQTS患者,也推荐应用β受体阻滞剂。
- 左房室瓣脱垂:对于有症状的左房室瓣脱垂患者,β受体阻滞剂通常作为首选药物。
β受体阻滞剂的主要禁忌症
β受体阻滞剂的主要不良反应
β受体阻滞剂是一类比较安全的药物,即使出现不良反应,只要及时发现并适当处理,很少会遗留长期或不可逆性严重损害。临床用于高血压、心力衰竭、冠心病等治疗。
- 中枢神经系统不良反应:多梦、幻觉、失眠、疲乏、眩晕以及抑郁等症状, 特别是脂溶性高的β受体阻滞剂, 易通过血脑屏障引起不良反应,如普萘洛尔。
- 消化系统不良反应:腹泻、恶心、胃痛、消化不良、便秘等消化系统症状。少数患者可致脏层腹膜纤维大量增生。
- 肢端循环障碍:少数患者出现四肢冰冷、发绀、脉搏消失, 以普萘洛尔发生率最高。
- 支气管痉挛:当服用非选择性β受体阻滞剂时, 由于β2受体被阻断, 使支气管收缩, 增加呼吸道阻力, 诱发或加重支气管哮喘的急性发作。
- 低血糖反应:β受体阻滞剂不影响胰岛素的降血糖作用, 但对正在使用胰岛素治疗的糖尿病患者, 使用β受体阻滞剂能延缓胰岛素引起低血糖反应后的血糖恢复速度, 即产生低血糖反应, 故糖尿病患者或低血糖患者应慎用此类药品。
- 心血管系统不良反应:临床较为常见的心血管系统不良反应有低血压、心动过缓等。
β1受体被阻断可能导致患者发生体位性低血压、心动过缓、传导阻滞、心力衰竭加重、掩盖患者的低血糖症状。这是由于药物对β1受体的阻断,降低了交感神经张力,减少心输出量、降低外周血管阻力,并抑制肾素-血管紧张素系统对心脏的负性频率和负性传导作用所致。老年患者或使用剂量较大时更易发生。
β2受体被阻断可能导致患者发生支气管痉挛、肢端循环障碍、加重外周循环性疾病,导致脂质代谢及性功能的不良影响。这是由于药物对β2受体的阻断,使支气管收缩,呼吸道阻力增加,诱发或加重支气管哮喘的急性发作,外周血管收缩、甘油三酯及低密度脂蛋白胆固醇升高,高密度脂蛋白胆固醇降低。这些不良反应在大剂量、长期用药时可能发生。
高亲脂性的β受体阻滞剂易通过血脑屏障,可能引起中枢神经系统不良反应,出现多梦、幻觉、失眠、疲乏、眩晕以及抑郁等症状。
因此,为增强降压效果、减少药物不良影响,临床上应尽量选择高β1受体选择性、高亲脂性,而无ISA的长效β受体阻滞剂,尤其是伴慢性阻塞性肺疾病(COPD)、外周动脉疾病(PAD)或糖尿病及中青年男性患者。
妊娠期及哺乳期妇女使用注意事项
临床常用的 β 受体阻滞剂有美托洛尔、阿替洛尔及艾可洛尔等。在美国食品药品监督管理局( FDA) 根据药品对妊娠妇女危害程度的分级标准中, 大部分药品属于 C 级或D 级。C 级药品是指动物研究证明其对胎儿有副作用( 致畸或杀死胚胎) , 但并未采用对照组妇女进行研究, 或者说没有对人和动物进行并行研究。该类药品只有在权衡了对孕妇的好处大于对胎儿的危害之后, 方可应用。D 级药品是指其有对胎儿危害性的明确证据, 尽管有危害性, 但孕妇用药后有绝对的好处( 如孕妇受到死亡的威胁或患有严重的疾病, 因此需用此药, 而应用其他药品虽然安全但无效) 。另外, 普萘洛尔、阿替洛尔可通过乳汁分泌, 故哺乳期妇女应慎用。
β受体阻滞剂临床运用
(1)把握用药时机,多靶点保护心血管
β受体阻滞剂在心血管疾病治疗中有非常广泛的应用,包括冠心病、心衰、心律失常、高血压、肥厚型心肌病等。β受体阻滞剂作用机制主要是拮抗儿茶酚胺类肾上腺素能递质毒性,尤其是拮抗β1受体介导的心脏毒性作用,能抑制肾素的释放和血管紧张素Ⅱ的产生,降低中枢缩血管活性。同时还可减慢心率、降低心肌收缩力和收缩压从而使心脏耗氧减少,改善冠状动脉血流灌注,抑制儿茶酚胺诱导的脂肪组织游离脂肪酸释放,提高心室颤动阈值,上调β肾上腺素能受体以及降低心肌氧化应激等。
如何把握β受体阻滞剂的用药时机,是一个非常重要的临床问题。
(2)心梗治疗:尽早应用
对于急性心肌梗死(心梗)的患者,在没有禁忌证的前提下,应在早期(出现症状后24小时内)应用β受体阻滞剂。其禁忌证包括心衰体征、低心排出量状态、心源性休克高风险、 PR 间期>0.24秒、Ⅱ度或Ⅲ度房室传导阻滞、活动性哮喘。对于急性心梗初始24小时内由于禁忌证未接受β受体阻滞剂治疗的患者,24小时后应重新评估其临床状态以决定是否可以应用该类药物。
(3)心衰治疗:先用ACEI还是β受体阻滞剂?
在慢性心衰患者中,通常血管紧张素转换酶抑制剂(ACEI)的应用先于β受体阻滞剂,这是基于临床研究的结果。多数心衰的临床试验都是在ACEI的基础上加用β受体阻滞剂。但是也有一个研究即心功能不全比索洛尔研究Ⅲ(CIBISⅢ)比较了慢性心衰患者先用ACEI或先用β受体阻滞剂,孰优孰劣。结果显示,先用β受体阻滞剂不劣于先用ACEI。这为心衰患者临床上先应用β受体阻滞剂提供了试验依据。
(4)用药前:排除水钠潴留状况
在心衰患者中应用β受体阻滞剂前应确保患者无明显的水钠潴留。这是由于β受体阻滞剂在短期内降低心肌收缩功能,在治疗前已有水钠潴留的患者应用该类药物容易出现症状恶化。存在水钠潴留的心衰患者,应先用利尿剂减轻水钠潴留至干体重或轻微水钠潴留状态,再开始应用β受体阻滞剂。用药过程中应密切监测患者体重及心衰症状和体征。临床上一部分慢性心衰患者的症状被忽略了,例如病例一,患者有胸闷伴水肿,虽然气急不是他的主诉,但实际上患者已经存在慢性心衰的症状。患者服用了β受体阻滞剂,导致短期内心衰症状的恶化。
一般来说,心衰患者出院前病情稳定情况下可以开始应用β受体阻滞剂。使用卡维地洛治疗心衰的研究(IMPACT-HF研究)和心衰入院患者初始治疗研究(OPTIMIZE-HF研究)的结果支持这点。 IMPACT-HF研究显示,与出院后开始应用β受体阻滞剂组相比,住院期间开始用药组60天后β受体阻滞剂的应用比例较高,且不良事件未明显增加。
心衰患者应用β受体阻滞剂应从最小剂量开始,例如卡维地洛3.125 mg bid,缓释美托洛尔12.5 mg或25 mg qd,比索洛尔1.25 mg qd。
(5)应用:尽量增至目标剂量
荟萃分析和观察性研究显示,β受体阻滞剂在收缩性心衰中的作用具有类效应。但目前的随机对照试验仅证实卡维地洛、比索洛尔和缓释美托洛尔能显著降低收缩性心衰患者全因死亡率和住院率,而其他β受体阻滞剂尚无足够随机对照试验的证据,因此2013年美国心脏病学会基金会/美国心脏学会(ACCF/AHA)指南推荐的β受体阻滞剂仍仅有这3种。对这3种β受体阻滞剂,目前尚无头对头比较研究。
此外,把握β受体阻滞剂的剂量对于心衰治疗也非常重要。临床上普遍存在的问题是,很多患者应用了β受体阻滞剂,但剂量未达标,常见的例如卡维地洛6.25 mg bid,此时药物益处未达最大化。
在患者耐受的前提下,要尽可能尝试增加β受体阻滞剂的剂量,使之达到目标剂量。在大规模临床试验中,多数收缩性心衰患者能够达到目标剂量,例如比索洛尔起始剂量为1.25 mg qd,每2周加倍,直至10 mg qd的目标剂量;缓释美托洛尔的目标剂量是200 mg qd;卡维地洛的目标剂量是25 mg bid。 临床实践中心衰患者的合并症可能高于临床试验中的患者,应用β受体阻滞剂能达到目标剂量的患者比例可能低于临床试验,但是也有相当一部分患者能达到目标剂量。
(6)撤药:逐步减量安全过渡
长期应用β受体阻滞剂突然停药可发生反跳现象,表现为高血压、心律失常和心绞痛恶化,这与长期治疗中 β肾上腺素能受体敏感性上调有关。
在高危患者中,突然撤除β受体阻滞剂是危险的,可能加重慢性心衰或心律失常,增加猝死的危险。因此,高危患者如果需要停用β受体阻滞剂,应逐步撤药,整个撤药过程至少持续2 周,每 2~3 日剂量减半,停药前的最后剂量至少持续 4天。若手术前要停用本药,必须至少在48 小时前停药。病例二是肥厚型心肌病患者,突然停用β受体阻滞剂导致了心律失常的发生。
应用β受体阻滞剂时出现水钠潴留和心衰恶化通常不是持续停用β受体阻滞剂的理由。多数情况下可以通过加强利尿扩血管药物治疗等改善血流动力学,而不需要持续停药,否则将升高患者死亡率。如果患者心衰恶化较重,例如存在低灌注、心动过缓或需要应用正性肌力药物时,可酌情暂时减量或停用β受体阻滞剂,待临床状况稳定后再加量或继续应用。
参看
参考文献
- β受体阻滞剂:如何把握最佳用药时机?中国医学论坛报
- 第八版《药理学》.人民卫生出版社
- 部分观点来自于专业医学网站医脉通
|
|||||||||||||||||
| 关于“Β受体阻滞剂”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |