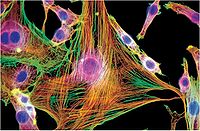
成纤维细胞
| A+医学百科 >> 成纤维细胞 |
成纤维细胞(fibroblast)成纤维细胞是疏松结缔组织的主要细胞成分,细胞呈梭形或扁的星状
,具有突起。根据不同的功能活动状态,将细胞分为成纤维细胞和纤维细胞二型:成纤维细胞乃是功能活动旺盛的细胞,细胞和细胞核较大,轮廓清楚,核仁大而明显,细胞质弱嗜碱性,具明显的蛋白质合成和分泌活动;纤维细胞(fibrocyte)功能活动不活跃,细胞轮廓不明显,核小着色深,核仁不明显,细胞质少。此二型细胞可互相转化。
目录 |
来源及特征
成纤维细胞:数目最多,胞体大,为多突的纺锤形或星形的扁平细胞,细胞核呈规则的卵圆形,细胞轮廓不清。
成纤维细胞摄取所需的氨基酸,如脯氨酸和赖氨酸等,在粗面内质网的核蛋白体上合成前α多肽链(proalpha polypeptide chain),多肽链输送到高尔基复合体后,组成前胶原分子(procollagen)。前胶原分子由分泌囊泡带到细胞表面,然后通过胞吐作用释放到细胞外。在前胶原肽酶催化下,将每一前α多肽链的尾段除去,成为原胶原分子(tropocollagen)。许多原胶原分子成行平行排列,结合成具有周期性横纹的胶原原纤维。由胶原原纤维互相结合形成胶原纤维。
是结缔组织中最常见的细胞,由胚胎时期的间充质细胞(mesenchymal cell)分化而来。在结缔组织中,成纤维细胞还以其成熟状态—纤维细胞(fibrocyte)的形式存在,二者在一定条件下可以互相转变。 不同类型的结缔组织含成纤维细胞的数量不同。通常,疏松结缔组织中成纤维细胞的数量比同样体积的致密结缔组织中所含成纤维细胞的数量要少,故分离培养成纤维细胞多以真皮等致密结缔组织为取材部位〔2,3〕。 成纤维细胞形态多样,常见的有梭形、大多角形和扁平星形等,其形态尚可依细胞的功能变化及其附着处的物理性状不同而发生改变。成纤维细胞胞体较大,胞质弱嗜碱性,胞核较大呈椭圆形,染色质疏松着色浅,核仁明显。电镜下,其胞质可见丰富的粗面内质网、游离核糖体和发达的高尔基复合体,表明它具有合成和分泌蛋白质的功能。成纤维细胞尚可合成和分泌胶原纤维、弹性纤维、网状纤维及有机基质。它合成的前胶原蛋白分子经内切酶作用,聚合和重排,可形成与成骨细胞合成分泌的胶原原纤维一样具有64nm(640Å)周期横纹的胶原原纤维,胶原原纤维经互相粘合形成胶原纤维。经检测,这两种细胞合成分泌的胶原纤维均是Ⅰ型胶原纤维,在形态和生化结构上完全相同〔4,5〕。 处于成熟期或称静止状态的成纤维细胞,胞体变小,呈长梭形,粗面内质网和高尔基复合体均不发达,被称为纤维细胞。在外伤等因素刺激下,部分纤维细胞可重新转变为幼稚的成纤维细胞,其功能活动也得以恢复,参与组织损伤后的修复。另外,在结缔组织中,仍保留着少量具有分化潜能的间充质细胞,它们在创伤修复等情况下可增殖分化为成纤维细胞。
创伤修复
一般创伤修复
各种创伤均会造成不同程度的细胞变性、坏死和组织缺损,必须通过细胞增生和细胞间基质的形成来进行组织修复。在此修复过程中,成纤维细胞起着十分重要的作用。以伤口愈合过程为例,成纤维细胞通过有丝分裂大量增殖,并从4~5天或6天开始合成和分泌大量的胶原纤维和基质成分,与新生毛细血管等共同形成肉芽组织,填补伤口组织缺损,为表皮细胞的覆盖创造条件。在伤口愈合中,成纤维细胞主要来源于真皮乳头层的局部成纤维细胞和未分化的间充质细胞,以及血管周围的成纤维细胞和周细胞。内脏损伤时,参与修复过程的成纤维细胞多来自间质和包膜,以及粘膜下或浆膜下层的结缔组织。有人认为创伤愈合过程中伤处聚集的大量成纤维细胞,一方面是由成纤维细胞通过分裂增殖而来,另一方面,更多地是由邻近的间充质细胞、纤维细胞和毛细血管周细胞等演变或游走到伤处。在创伤修复的后期,成纤维细胞通过分泌胶原酶参与修复后组织的改建。在某些病理条件下,以成纤维细胞为主要细胞成分的肉芽组织或增生组织块还可以在非骨组织内发生钙化,引起异位骨化(ectopic ossification)。但对于异位骨化的参与细胞及其机制尚不十分清楚,未分化间充质细胞、成纤维细胞、内皮细胞和毛细血管周细胞等可划归为诱导性骨祖细胞的细胞都有可能参与这一过程
骨创伤修复
最简单和常见的骨创伤即是骨折,其愈合过程须经过炎性反应、清扫、纤维骨痂和骨性骨痂4个阶段。不同阶段参与的细胞主体不同。成纤维细胞从骨折第3天起就出现于骨折局部血肿中,骨折后5天即在机化血肿及骨折断端的间隙及其周围大量存在,是参与纤维骨痂阶段的主要细胞成分。在此阶段成纤维细胞一方面大量分裂增殖,一方面又合成和分泌大量Ⅰ型胶原,使肉芽组织逐步变成疏松的结缔组织,将骨断端包围起来,形成接合两骨折断端的巨大的纤维骨痂。然而,这种由无数成纤维细胞和丰富的肉芽组织为主体构成的纤维结缔组织却不会演变为在其它组织创伤修复时常见的瘢痕组织,而是通过钙盐结晶在其内部不断沉积,逐渐演变为骨性骨痂,使骨折局部的修复达到骨性愈合,恢复骨组织的结构。此时,骨折愈合部只有骨组织而不再存在成纤维细胞。
培养
成纤维细胞的分离培养一开始并不涉及成骨作用,而主要是用于研究细胞的老化、各种外来因子对细胞的损伤、细胞在体外条件下的恶性转化、以及某些先天性代谢异常、酶缺陷等。由于皮肤成纤维细胞易于获取,又易于在体外生长,故目前皮肤成纤维细胞培养已在基础医学和临床医学研究中得到较广泛的运用,其分离培养技术已相对成熟,对其体外生长规律也有了较全面的认识。
成纤维细胞的原代培养可用酶消化法或组织块法,其中组织块法又因其操作简便、条件易于控制而应用更为普遍。通常,以酶消化法获得的成纤维细胞悬液在接种后5~10min即可见细胞以伪足初期附着,与底物形成一些接触点;然后细胞逐渐呈放射状伸展,胞体的中心部分亦随之变扁平;最快者大约在接种后30min,细胞贴附底物即较为完全,呈现成纤维细胞的形态。采用组织块法则大约在接种后2~3天[2,3]到1周左右,在接种的皮肤组织块周围长出细胞。待细胞融合成片,铺满培养容器底壁大部分时即可进行传代。一般都采用胰蛋白酶(trypsin),将成纤维细胞从底壁消化下来后分瓶作传代培养。成纤维细胞在体外培养条件下能保持良好的分裂增殖能力。细胞分裂时变为球形;分裂后又平铺在附着物的表面成为有突起的扁平细胞。体外培养的成纤维细胞,其生命期限与物种等因素有关。例如:人胚成纤维细胞约可培养50代;恒河猴皮肤成纤维细胞能传代超过40代;鸡胚成纤维细胞则只有少数能培养30代;而小鼠成纤维细胞多数只能生长8代左右。另外,从老年个体取得的成纤维细胞的寿命要比取自年轻者短。由于在细胞传代和进行体外培养时,细胞的生物学特性会逐渐发生一些不同于体内的改变,故通常只将前10代视这正常细胞,可在此时将生长旺盛的成纤维细胞冻存起来,以备将来复苏使用,这在将培养的细胞由动物实验向人体实验过渡的过程中必须给予足够的重视。
展望
尽管成纤维细胞受哪些因素诱导可以产生成骨作用、这些因素的诱导方式及其机制如何以及成纤维细胞在骨形成中是否分化为成骨细胞等等问题尚未完全解决,但成纤维细胞经诱导可以形成骨组织这一现象已逐渐为广大科学工作者所接受。由于成纤维细胞直接参与了骨折愈合过程中纤维性骨痂的形成,其自身又具备被诱导成骨的能力,可以设想,利用成纤维细胞分布广泛、取材方便、对机体损伤较小、体外培养容易成活、增生繁殖较快等较其它具有成骨作用的细胞(如骨膜成骨细胞、骨髓基质细胞等)优越之处,在体外大量培养扩增成纤维细胞,并施以有效的诱导因素(如上皮细胞、TNG-α和BMP等)使其具备成骨效能,然后与合适的生物材料载体复合,同时使该复合体在体外或体内保持良好的成骨能力并进行一定程度的成骨,则有望获得具有一定的生物力学支撑强度而成骨作用又保持活跃的“活骨”复合体,用以替代自体骨或异体骨回植体内治疗难以自身修复的较大的骨缺损,这无疑将为骨缺损的修复治疗开辟一条新的有辉煌前景的道路。在组织工程技术和生物材料科学已有较大发展的今天,这一设想是极有可能实现的。当然,从目前所处的实验阶段过渡到临床应用尚有很大一段距离,需要解决的问题还很多,而且随着研究的展开和深入,问题可能还会越来越多,但这确实是一项很有临床应用价值和社会、经济效益的重大课题,值得广大基础医学工作者和临床科研人员为之而努力。
| 关于“成纤维细胞”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |