医用化学/碳原子的sp3、sp2和sp杂化轨道
| 医学电子书 >> 《医用化学》 >> 有机化合物概述 >> 碳原子的sp3、sp2和sp杂化轨道 |
| 医用化学 |
|
|
|
杂化轨道理论已在第四章 讨论过了。本节仅对碳原子的杂化轨道作一简单介绍。
甲烃分子中的碳原子是sp3杂化的,杂化后的四个sp3轨道构成109°28′的夹角[图10-1(a)]。在甲烷分子中,碳原子的四个sp3杂化轨道分别与四个氢原子1s轨道重叠形成键角为109°28′的正四面体分子[图10-1(b)]。
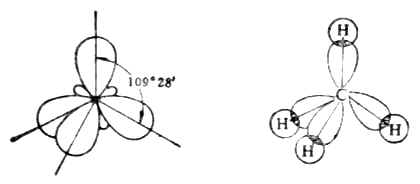
(a) (b)
图10-1 四个sp3杂化轨道和甲烷
成键情况
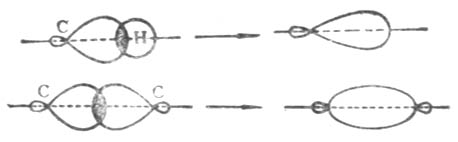
图10-2 由sp3-s和sp3-sp3形成的碳氢o键和碳碳o键
烷烃分子中的碳氢键和碳碳键是碳原子的一个sp3杂化轨道与氢原子的1s轨道或另一个碳原子的一个sp3杂化轨道重叠而成(图10-2)。这样形成的碳氢单键和碳碳单键,其电子云具有圆柱状的轴对称,叫做σ键。由于它是轴对称的,所以用单键相连的碳氢原子或碳碳原子可以围绕轴自由旋转。
乙烯分子中的碳原子与甲烷的碳原子不同,它是sp2杂化的。也就是说,碳原子的三个p轨道中的两个参与杂化,而另一个p轨道未参与杂化。杂化后生成了三个相同的sp2轨道。这三个轨道轴在同一个平面上,互成120°的角。另一个未参与杂化的p轨道的对称轴垂直于这个平面。
在乙烯分子中,碳原子的三个sp2杂化轨道中的两个同氢原子的1s轨道重叠形成碳氢σ键。未参与杂化的两个p轨道用侧面互相重叠形成一个π键(图10-3)。
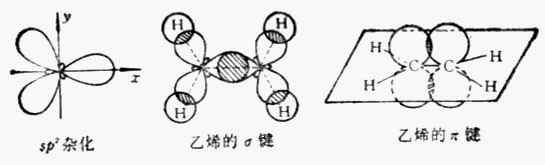
图10-3 sp杂化轨道及乙烯的o键和π键
所以,双键是由一个σ键和一个π键组成的。
碳原子的2s轨道同一个2p轨道杂化,形成两个相同的sp杂化轨道。它们对称地分布在碳原子的两侧,二者之间的夹角为180°。乙炔分子中的键就是由sp杂化轨道形成的。碳原子的一个sp杂化轨道同氢原子的1s轨道形成碳氢σ键,另一个sp杂化轨道与相邻的碳原子的sp杂化轨道形成碳碳σ键,组成直线结构的乙炔分子。没有参与杂化的两个p轨道与另一个碳的两个p轨道相互平行,且“肩并肩”地重叠,形成两个相互垂直的π键(图10-4)。
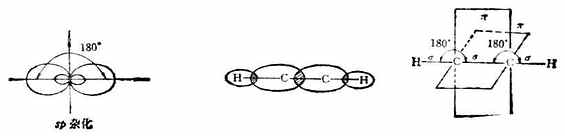
图10-4 sp杂化轨道及乙炔的o键和π键
| 关于“医用化学/碳原子的sp3、sp2和sp杂化轨道”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |