叠氮甲烷
| A+医学百科 >> 叠氮甲烷 |
| 叠氮甲烷 | |
|---|---|
 |
|
| 别名 | 甲基叠氮化物 |
| 识别 | |
| PubChem | 79079 |
| ChemSpider | 71411 |
| SMILES |
|
| 性质 | |
| 化学式 | CH3N3 |
| 摩尔质量 | 57.05 g·mol⁻¹ |
| 爆炸性 | |
| 撞击感度 | 高 |
| 摩擦感度 | 高 |
| 危险性 | |
| 主要危害 | 有害,易爆炸 |
| 相关物质 | |
| 相关化学品 | 叠氮酸、叠氮化氯、叠氮乙烷 |
| 若非注明,所有数据均出自一般条件(25 ℃,100 kPa)下。 | |
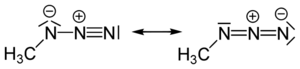
叠氮甲烷(CH3N3)是烷基叠氮化物的一种,它们都属于叠氮酸的共价型衍生物。叠氮甲烷是一种直线型分子。根据共振式,中间的氮原子的两对成键电子显然是直线形排列的,但与甲基相连的氮原子却有三对孤对电子:H3C-N=N+=N- ⇔ H3C-N--N+≡N 。[1]
它可以由叠氮化钠的甲基化反应制得。该物质最早于1905年制得。[2] 它以如下的一级反应分解:CH3N3 → CH3N + N2。[3]
无生源论认为,叠氮甲烷可能是在星际冰中由高能银河宇宙射线和光子合成分子的前体之一。[4]
安全措施
叠氮甲烷在常温时稳定但加热时可能爆炸。[5] 汞的存在将增加它对震动和火花的敏感度。它与丙二酸二甲酯、甲醇钠、汞、甲醇、叠氮化钠、硫酸二甲酯、氢氧化钠、叠氮酸不能共存。加热分解时产生有毒的氮氧化物气体。
参考资料
- ↑ Pauling, Linus, Brockway, O.; The Adjacent Charge Rule and the Structure of Methyl Azide, Methyl nitrate, and Fluorine nitrate; JACS, 1937, 59 (1), pp 13-20 DOI:10.1021/ja01280a005
- ↑ Dimroth, O. and Wislicenus, W.; Chemische Berichte ; 38, 1573 (1905)
- ↑ O'Dell, M.S. and Darwent B. Thermal decomposition of methyl azideCanadian Journal of Chemistry, 48, 1140 (1970)
- ↑ Alfredo Quinto-Hernandez and Alec M. Wodtke, Department of Chemistry and Biochemistry, University of California, Santa Barbara; Chris J. Bennett, Y. Seol Kim, and Ralf I. Kaiser; Department of Chemistry, University of Hawaii at Manoa; On the Interaction of Methyl Azide (CH3N3) Ices with Ionizing Radiation: Formation of Methanimine (CH2NH), Hydrogen Cyanide (HCN), and Hydrogen Isocyanide (HNC) ; Journal of Physical Chemistry DOI: 10.1021/jp103028v Publication Date (Web): December 17, 2010
- ↑ Bretherick's handbook of reactive chemical hazards; edited by P. G. Urben
- Graner, G., Hirota, E., Iijima, T., Kuchitsu, K., Ramsay,D. A., Vogt, J., Vogt,N.: CH3N3 Methyl azide. Kuchitsu, K. (ed.). SpringerMaterials - The Landolt-Börnstein Database [1] DOI: 10.1007/10653318_320
- NIST Webbook
参考来源
出自A+医学百科 “叠氮甲烷”条目 http://www.a-hospital.com/w/%E5%8F%A0%E6%B0%AE%E7%94%B2%E7%83%B7 转载请保留此链接
| 关于“叠氮甲烷”的留言: | |
|
目前暂无留言 | |
| 添加留言 | |